21 CFR Part 11準拠のためのCytExpert解析ツール
品質管理に関するデータやFDAに報告されるデータを保存しているすべてのコンピュータシステムは、21 CFR Part 11に準拠していなければなりません。本規則は、「電子記録・電子署名」が信頼に値する確実なものであり、従来の「紙媒体の記録」と同等であるとみなすための基準を定めています。
21 CFR Part 11とは、電子記録・電子署名の使用に関する米国食品医薬品局(FDA)のガイドラインを定める米国連邦規則(CFR)の条項のことです。医薬品、生物学的製剤、医療機器、および食品(ヒトおよび動物用)といった広範な業界が、本項による規制を受けています。これらの部門に属し米国で営業している企業、原材料および成分を製薬会社に供給する業者、分析業務を受託する研究所はすべて、電子記録・電子署名が信頼に値し、確実であることを保証できるよう、業務を行わなければなりません。
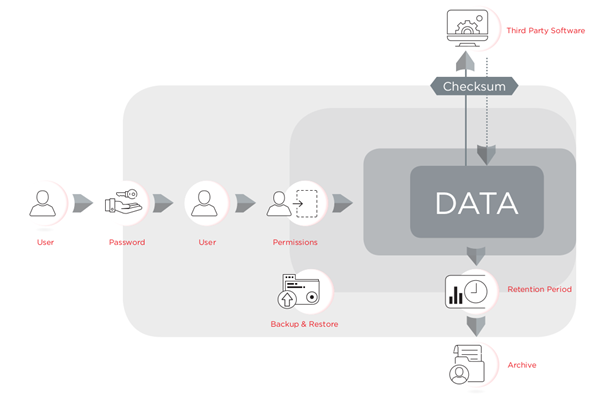
本条項では、組織に以下の3つのレベルの管理を行うよう要求しています。すなわち、電子記録に関する方針などの運営上の管理、システムの使用に関するSOPなどの手順に関する管理、および電子記録・電子署名の信頼性と完全性を保証するソフトウエアに組み込む機能に関する技術的管理です。ソフトウエアを21 CFR Part 11の技術的管理基準に準拠するようデザインすることはできますが、ラボの担当者は方針と手順を提示し、その適切な使用を保証する責任を負っており、ラボのプロセスが確実に本条項に準拠するようにしなければなりません。CytoFLEXフローサイトメーターでは、CytExpertのv2.3以降に搭載されている電子記録管理ツールが利用可能です。このソフトウェアは容易に21 CFR Part 11に準拠できるよう設計されています。CytoFLEX用解析ソフトウエアCytExpertはパスワードで保護されており、装置の運転を管理し、チェックサムと監査証跡を用いたデータの完全性を管理・保護し、署名、署名階層およびアーカイブを用いた文書管理などの機能を提供します。